Quando as pessoas começaram a considerar o mundo em escalas menores, por exemplo, elétrons orbitando o núcleo de um átomo, elas perceberam que as coisas ficam muito estranhas e que as leis de Newton não se aplicam mais. Para descrever este minúsculo mundo você precisa da mecânica quântica, uma teoria desenvolvida no início do século XX. A equação central dessa teoria, que é o análogo da segunda lei de Newton, é chamada de equação de Schrödinger.
Mecânica: Newtoniana x Quântica
Na mecânica clássica (Newtoniana), descrevemos o estado de um sistema físico usando a posição e o momento. E usamos as leis de Newton para descrever a evolução dinâmica de um sistema. Na mecânica quântica a posição e o momento não são mais as variáveis certas para descrever o sistema. O problema é que os objetos que a mecânica quântica tenta descrever nem sempre se comportam como minúsculas partículas. Às vezes, é melhor pensar neles como ondas. Ou seja, os objetos ora se comportam como ondas ora como partículas (temos então, uma dualidade onda-partícula).
A dualidade onda-partícula
Uma das demonstrações mais famosas da dualidade onda-partícula é o experimento da dupla fenda (Figura). Nele, elétrons são disparados um de cada vez em uma tela contendo duas fendas. Atrás da tela, há um detector que pode detectar para onde vão os elétrons que passaram pelas fendas.
Se os elétrons se comportassem como partículas, esperaríamos que eles se acumulassem em torno de duas linhas retas atrás das duas fendas (como na imagem inferior da Figura 1). Mas o que você realmente vê na tela do detector é um padrão de interferência: o padrão que você obteria se os elétrons fossem ondas (igual está demonstrado da imagem superior à esquerda). Ou seja, a onda passando por ambas as fendas ao mesmo tempo e interferindo consigo mesma, se espalhando do outro lado. É um resultado muito estranho, mas que foi replicado muitas vezes (simplesmente temos que aceitar que é assim que o mundo funciona).
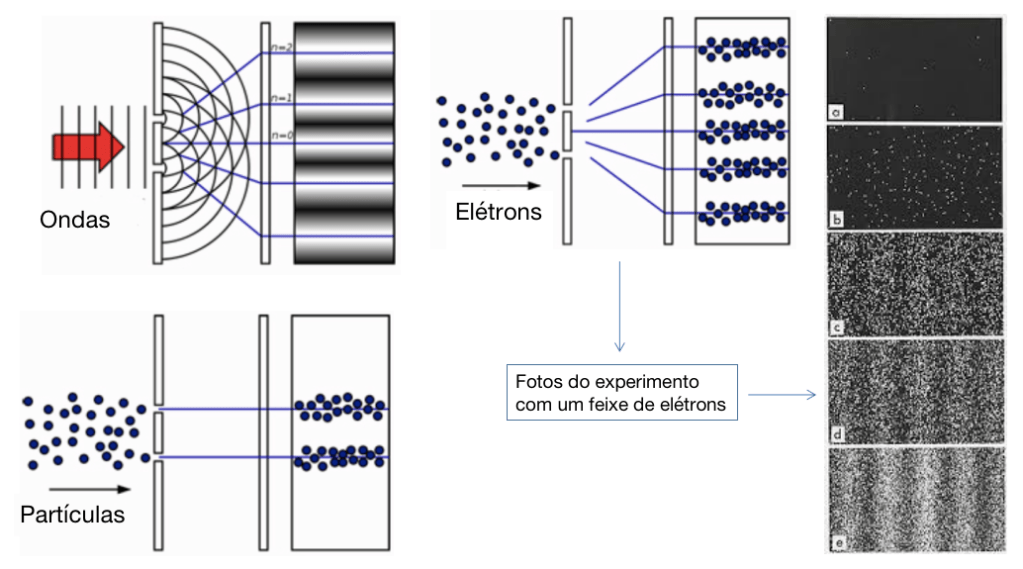
Figura: Experimento de Dupla Fenda realizado com ondas, partículas e elétrons. Os cinco padrões de interferência apresentados no canto direito representam uma foto real do experimento com elétrons.
Por que devemos acreditar nesta configuração bastante fantástica? De onde vem a equação de Schrödinger? Como Schrödinger a derivou? O famoso físico Richard Feynman considerou isso uma pergunta fútil. Não é possível derivá-la de qualquer coisa que você conhece. Saiu da mente de Schrödinger.
No entanto, a equação se manteve coerente em todos os experimentos até agora. “É a equação mais fundamental da mecânica quântica”. O primeiro sucesso da equação, foi descrever o espectro de energia discreto do átomo de hidrogênio. Antes, de acordo com o modelo atômico de Ernest Rutherford, a frequência da radiação emitida por átomos como o hidrogênio deveria variar continuamente. Experimentos mostraram, no entanto, que não: o átomo de hidrogênio apenas emite radiação em certas frequências (ou seja, sua energia é quantizada).
Em 1913, Niels Bohr apresentou um novo modelo atômico no qual os elétrons são restritos a certos níveis de energia. Schrödinger aplicou sua equação ao átomo de hidrogênio e descobriu que suas soluções reproduziam exatamente os valores numéricos de níveis de energia estipulados por Bohr (veja mais em nosso artigo sobre o modelo quântico para o átomo de hidrogênio).
Fonte: Disponível em <https://plus.maths.org/content/schrodinger-1> acesso em novembro de 2020, <https://journals.aps.org/prl/abstract/10.1103/PhysRevLett.100.073003> acesso em 2023.

Deixe um comentário