O átomo de hidrogênio é o sistema ligado mais simples que ocorre na natureza. Consiste de um núcleo carregado positivamente e um elétron carregado negativamente, conectados pela força de atração coulombiana, se movendo segundo o potencial:
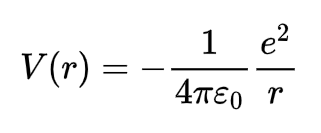
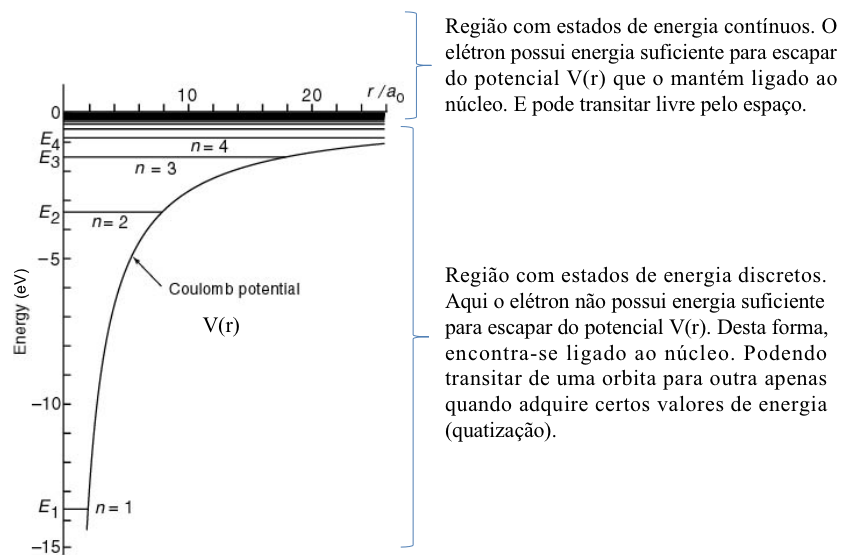
Figura 1: A figura representa o potencial Coulombiano para o átomo de hidrogênio (interação entre o núcleo e o elétron). A abscissa denota a coordenada de posição do elétron (a distância entre o próton e o elétron), r , em unidades de raio de Bohr .
Por ser o sistema ligado mais simples encontrado na natureza, o átomo de hidrogênio é um dos poucos sistemas reais na qual pode ter sua equação de ‘‘movimento’’ resolvida analiticamente.
Na mecânica clássica, a equação de movimento é a famosa segunda lei de Newton (F = ma). Ela é utilizada para prever matematicamente o movimento de um sistema clássico (como um carro se movendo) no decorrer do tempo.
Na mecânica quântica, o análogo à segunda lei de Newton é a equação de Schrödinger (1925). Ela descreve como sistemas quânticos (átomos, moléculas e partículas subatômicas) variam no tempo (ou seja, descreve o estado quântico de um sistema).
- Equação de Schorodinger dependente do tempo (ESDT)
A equação de Schorodinger dependente do tempo (ESDT), em 3 dimensões, em coordenadas esféricas (r, θ, φ) para uma partícula sujeita a um potencial V(r) é dada por:
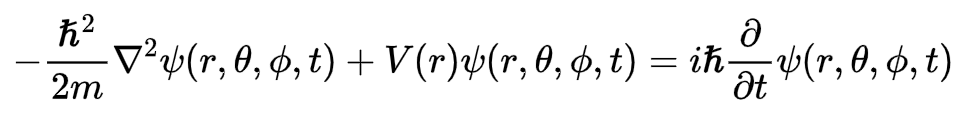
Solução geral:
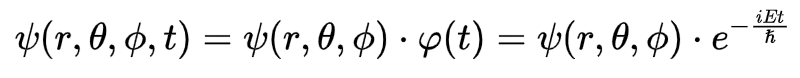
Solução da parte temporal:
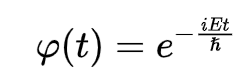
A solução da parte espacial também é chamada de autofunção (ou autofunções, se existirem mais de uma solução possível). Em especial, para o átomo de hidrogênio existem infinitas soluções possíveis, ou seja, infinitas autofunções e para obte-las é necessário resolver a Equação de Schorodinger independente do tempo (ESIT).
- Equação de Schorodinger independente do tempo (ESIT)
A equação de Schorodinger independente do tempo (ESIT), em 3 dimensões, em coordenadas esféricas (r, θ, φ) para uma partícula (elétron) sujeita a um potencial V(r) é dada por:
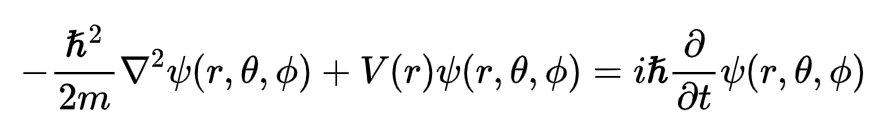
Solução (parte espacial):
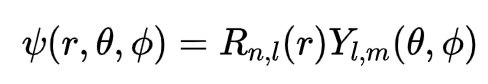
R(r) é a solução da parte radial, escrita em termos de polinômios de Laguerre e Y(θ, φ) é a solução da parte angular, escrita em termos de harmônicos esféricos. Todos os cálculos para chegar na solução da ESIT são realizados em outro post (clique aqui para saber mais). Note que toda a base da mecânica quântica é puramente matemática e estatística, aliada a experimentos que comprovam tais modelos algébricos. Desta forma, a compreensão dos conceitos e modelos se torna muito difícil e é natural não compreender. O estranho seria compreender tudo!
Os números quânticos n, l, m surgem naturalmente da solução matemática da ESIT, como também a quantização do momento angular (ver explicação aqui). E as autofunções dependem desses três números quânticos, pois são produtos das três funções, R(r). Ф(φ). Θ(θ), onde:
n = 1, 2, 3, … é o número quântico principal.
l = 0, 1, 2, 3, …, n-1. é o número quântico azimutal.
m = – l, … , -1, 0, 1, …, + l. é o número quântico magnético orbital.
ms = +1/2, – 1/2. é o número quântico magnético de spin.
Conforme listado abaixo (Tabela 1), para cada valor de n, existem n2 autofunções degeneradas, ou seja, com o mesmo valor de energia En.
Tabela 1: A Tabela 1 representa em ordem de proximidade com o núcleo atômico, os primeiros orbitais (s, p), números quânticos (n, l, m), autofunções, energias (ou autovalores de energias) e degenerescência.
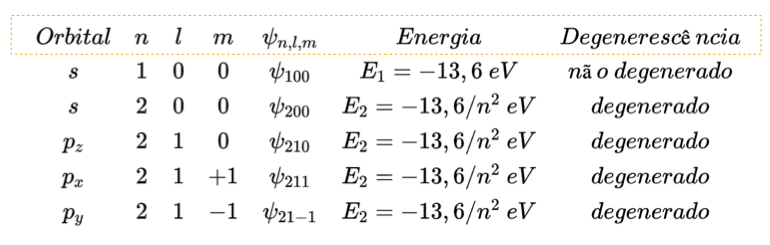
Note que, na Tabela 1, as quatro ultimas autofunções são degeneradas, ou seja, possuem o mesmo valor de energia (já que o valor de n é o mesmo). Isso ocorre devido a simetria esférica do átomo. Uma quebra de simetria, resulta numa quebra de degenerescência. Isso ocorre, por exemplo, com a aplicação de um campo magnético externo ao átomo. Assim, o campo magnético aplicado, perturba os níveis de energia, deslocando-os levemente para cima ou para baixo uns em relação aos outros.
A Figura abaixo mostra uma representação artística dos orbitais 1s, 2s, e 2p ( 2px, 2py , 2pz). A nomenclatura de orbitais (s, p, d, f, …) é muito usada em estudos de espectroscopia atômica e molecular, na qual é discutido em outro post.
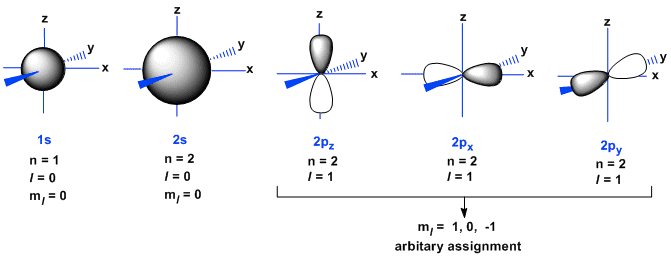
Fontes: Robert Eisberg, Física Quântica – Átomos, Moléculas, Sólidos, Núcleos e Partículas, 1º edição (1979). | Disponível em <http://www.chem.ucalgary.ca/courses/350/mechanistic_etext/Ch01/ch1-1-2.html> | <https://journals.aps.org/prl/abstract/10.1103/PhysRevLett.110.213001> acessado em 2020

Deixe um comentário