Quando um átomo absorve um quantum de energia, diz-se que ele está em um estado excitado em relação ao seu estado fundamental (aquele de menor energia). Quando um átomo excitado retorna ao estado fundamental, ele emite luz. Quando essa luz é observada através de um espectroscópio (Figura 1), as imagens são uma série de linhas coloridas. As várias cores correspondem à comprimentos de onda definidos, e a série de linhas é chamada de espectro de linhas. O espectro de linha de cada elemento é tão característico desse elemento (é único para cada átomo, molécula, composto, etc…) que pode ser usado para identificá-lo.
Mas como excitar um átomo? Ou seja, como faze-lo absorver energia para que possamos observar seu espectro?
Bom, primeiro é necessário popular os estados de maior energia. Isso é feito passando uma descarga elétrica através de um tubo contendo gás (nesse caso, gás hidrogênio), conforme mostrado na Figura 1. Assim, o elétron ganha energia, salta para um estado excitado e emite um fóton ao retornar para o seu estado fundamental.
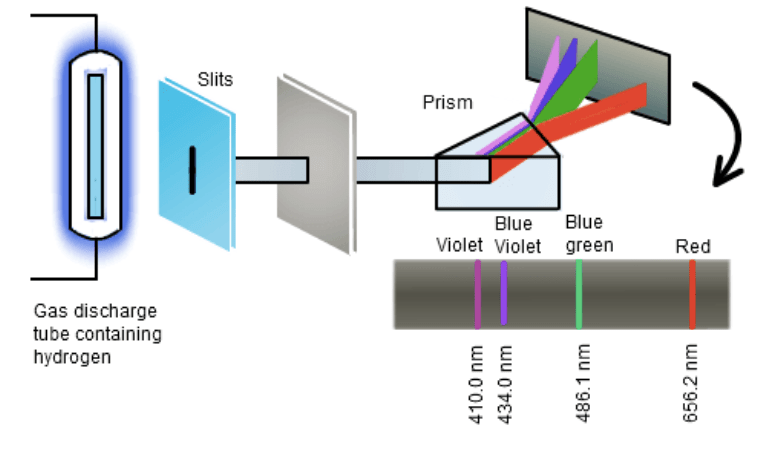
Figura 1: Imagem ilustrando como ocorre o processo de absorção/emissão e a observação dessa luz emitida através de um espectro de emissão (para o átomo de hidrogênio). Fonte.
- Séries de linhas espectrais:
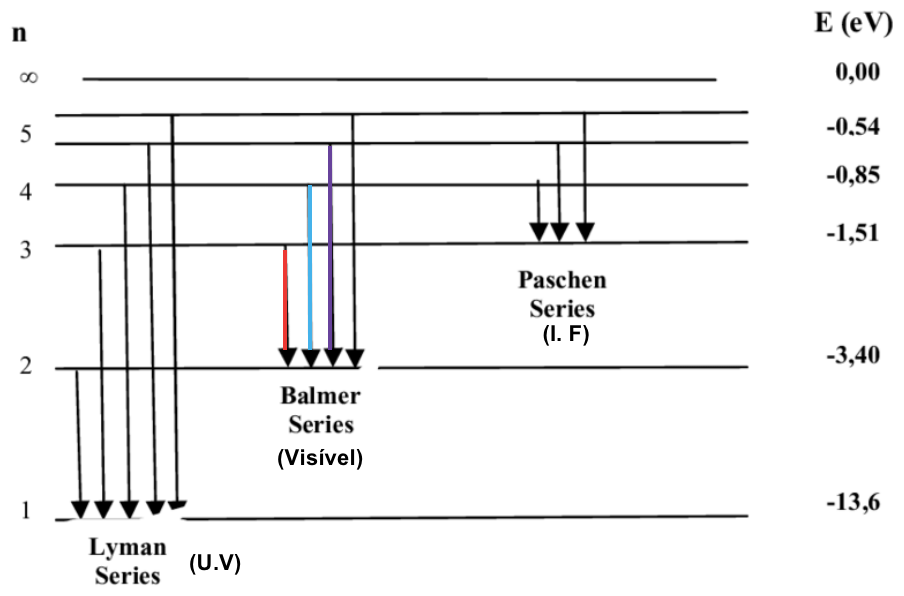
Os processos de emissão ou absorção no hidrogênio dão origem a séries, que são sequências de linhas correspondentes às transições atômicas (absorção ou emissão). A Série Balmer envolve transições que começam (para absorção) ou terminam (para emissão) com o primeiro estado excitado do hidrogênio (n=2). Enquanto a Série Lyman envolve transições que começam ou terminam com o estado fundamental do hidrogênio (n = 1). A imagem adjacente ilustra as transições atômicas que produzem essas séries.
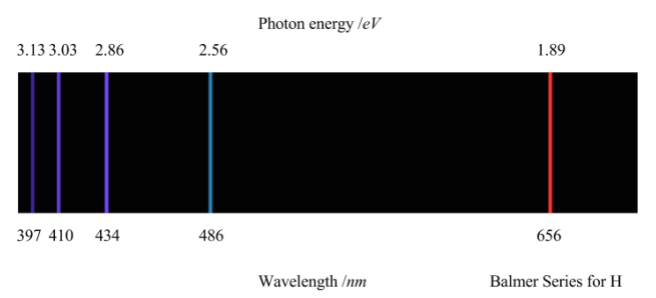
O espectro visível do hidrogênio corresponde a série de Balmer e está ilustrado abaixo. Note que os valores numéricos de energia (em eV) correspondentes às transições atômicas desta série são obtidos calculando os valores de energia entre os estados na qual o elétron transitou (por exemplo, entre os níveis n2 e n3, na série de Balmer, temos: 3,40 – 1,51 = 1,89 eV, conforme está indicado pela linha vermelha na figura abaixo).
Em 1914, Niels Bohr propôs uma teoria para o átomo de hidrogénio. De acordo com esta teoria, os comprimentos de onda do espectro do hidrogênio poderiam ser calculados pela seguinte fórmula conhecida como fórmula de Rydberg.
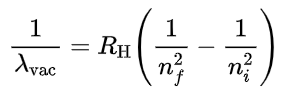
Onde:
λvac é o comprimento de onda da luz emitida no vácuo característico de cada elemento,
RH é a constante de Rydberg (para o hidrogênio é 109.677,581 cm-1)
ni e nf são números inteiros, sendo: nf < ni
Aqui abordamos um pouco sobre o espectro do átomo de Hidrogênio que se enquadra dentro do estudo da espectroscopia atômica de modo geral. Em outra postagem, falamos sobre a espectroscopia atômica e as diferenças entre espectroscopia atômica e molecular.
Fontes: Robert Eisberg, Física Quântica – Átomos, Moléculas, Sólidos, Núcleos e Partículas, 1º edição (1979). |Disponível em: <http://eilat.sci.brooklyn.cuny.edu/cis1_5/old%20hws/hw2d_c.htm> , <https://collegedunia.com/exams/hydrogen-spectrum-series-line-spectrum-hydrogen-wavelength-chemistry-articleid-566> acesso 10/10/2023.

Deixe um comentário