Ambos fenômenos, Raman e Fotoluminescência, podem ocorrer quando incide-se luz laser sobre uma amostra.
Espectroscopia Raman
No espalhamento Raman (1930 – Nobel Física), um laser incide perpendicularmente sobre uma amostra e é espalhado elástica ou inelásticamente. No caso elástico, os fótons espalhados têm frequência igual a dos incidentes, originando o efeito Rayleigh, na qual não fornece informações muito úteis sobre as características da amostra. Nos caso inelástico, os fótons espalhados têm frequência diferente das incidentes, originando o efeito Raman. Os fótons espalhados podem apresentar frequência menor (anti-Stokes) ou maior (Stokes) que a freqüência da radiação incidente, conforme ilustrado na Figura 1.
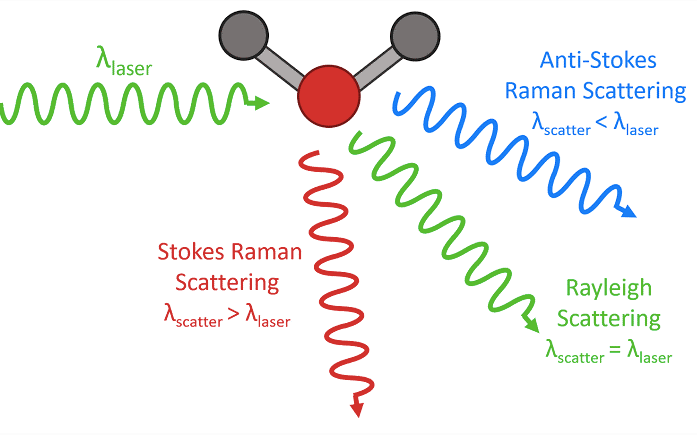
Figura 1: Efeitos que ocorrem em uma molécula ao ser incidida por luz laser. Fonte: https://www.insightsonindia.com/2020/07/07/what-is-raman-spectroscopy/
Durante este processo a molécula (normalmente no estado líquido) muda seu estado rotacional-vibracional, e no caso de sólidos cristalinos são promovidas vibrações na sua rede cristalina. Esta técnica é não destrutiva, não necessita vácuo e se aplica a quase todos os tipos de materiais: orgânicos, inorgânicos, amorfos ou cristalinos (esse é um diferencial em relação a difração de raios-X que é utilizada apenas em materiais cristalinos).
A espectroscopia Raman investiga a estrutura química e cristalina de um material e fornece informações sobre:
- Estrutura química e identidade do material
- Fase e polimorfismo
- Estresse/tensão intrínseca na rede cristalina
- Contaminação e impureza
Normalmente, um espectro Raman é uma impressão digital química distinta para uma molécula ou material específico e pode ser usado para identificar rapidamente o material ou distingui-lo de outros. Bibliotecas espectrais Raman são frequentemente usadas para identificação de um material com base em seu espectro Raman – bibliotecas contendo milhares de espectros são rapidamente pesquisadas para encontrar uma correspondência com o espectro do analito.
Fotoluminescência: fluorescência X fosforescência
Fotoluminescência (abreviada como PL ) é a emissão de luz, emitida por um material, após a absorção de fótons (radiação eletromagnética). É uma das muitas formas de luminescência (emissão de luz) e é iniciada por fotoexcitação (ou seja, fótons que excitam elétrons para um nível de energia mais alto). Compreende dois processos: fluorescência (decaimento rápido) e fosforescência (decaimento lento). A diferença entre os mecanismos pelos quais ocorrem os fenômenos de fluorescência e fosforescência estão demonstrados no diagrama de Jablonski (Figura 2). O diagrama de Jablonski é utilizado em espectroscopia de fluorescência para ilustrar os estados excitados de uma molécula e as transições radiativas e não radiativas que podem ocorrer entre eles.
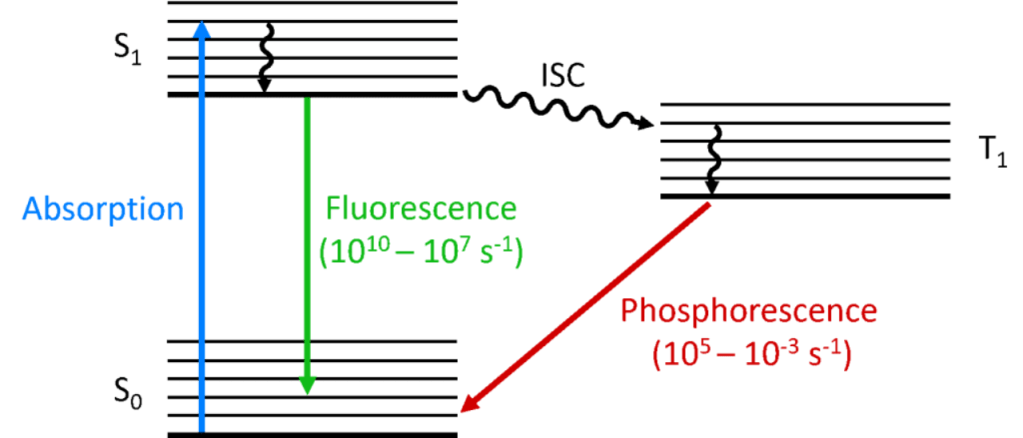
Figura 2: Diagrama de Jablonski com os fenômenos de fluorescência e fosforescência. Fonte: https://www.edinst.com/us/blog/photoluminescence-differences/.
Quando um fóton é absorvido pela molécula, um dos elétrons é promovido para um nível de energia mais elevado e a molécula fica agora em um estado excitado. O estado fundamental de uma molécula é (quase) sempre um estado singleto (S0) e devido à conservação do momento angular o estado fotoexcitado também deve ser um estado singleto (S1). O decaimento do estado S1 de volta ao S0 é uma transição permitida (uma vez que ambos os estados têm a mesma multiplicidade de spin), resultando em fotoluminescência imediata que ocorre na escala de tempo de picossegundos a nanossegundos e é chamada de fluorescência (decaimento rápido) (Este decaimento está representado na cor verde da Figura 2).
Alternativamente, a molécula pode sofrer cruzamento intersistemas (ISC) para o estado tripleto excitado (T1). O ISC normalmente ocorre em moléculas com um alto grau de acoplamento spin-órbita, o que permite a conversão entre os estados. A força do acoplamento spin-órbita aumenta com a massa do átomo e, portanto, as moléculas fosforescentes devem conter metais pesados, como európio e irídio. O decaimento do estado T1 de volta para S0 é uma transição proibida, uma vez que os estados possuem diferentes multiplicidades de spin, devido à conservação do momento angular. No entanto, o acoplamento spin-órbita relaxa esta restrição e uma transição radiativa torna-se possível. Uma vez que é “proibida”, a fotoluminescência resultante da transição T1 para S0 ocorre numa escala de tempo muito mais lenta, de microssegundos a milhares de segundos, e é chamada de fosforescência (decaimento lento) (Este decaimento está representado pela cor vermelha na Figura 2).
A espectroscopia de fotoluminescência em semicondutores pode fornecer informações a respeito de defeitos na rede cristalina (como vacâncias, estresse na rede, etc). Em semicondutores, a medida que a temperatura diminui, a intensidade do espetro PL aumenta, tornando seus picos mais definidos. Isso ocorre pois quando a agitação térmica aumenta, o material emite energia referente a vários níveis, mascarando a energia emitida pelo fenômeno de fotoluminescência (que fica sobreposta pela emissão referente a energia térmica emitida pelo material). Desta forma, quanto mais baixa a temperatura, mais provável observar no espectro PL picos referentes às energias de transições que ocorrem próximas ao estado fundamental. Sendo assim, a fotoluminescência é caracterizada pela emissão não térmica de luz.
Fontes: Disponível em <https://www.horiba.com/bra/scientific/technologies/raman-imaging-and-spectroscopy/raman-spectroscopy/> <https://www.edinst.com/us/blog/photoluminescence-differences/> <https://en.wikipedia.org/wiki/Photoluminescence> <https://www.edinst.com/us/blog/jablonski-diagram-2/> acesso em 2023.

Deixe um comentário